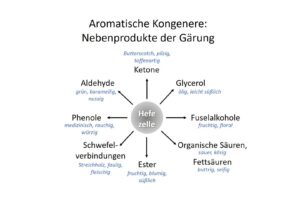
Was passiert eigentlich bei der Destillation wirklich in der Brennblase? Wer denkt, dass dabei lediglich das schwere flüchtige Wasser von dem leichtflüchtigen Alkohol Ethanol getrennt wird, hat nur die halbe Wahrheit im Glas. Denn im Inneren der Brennblasen – die sogenannten Pot Stills –, wo sich Dampf und Metall begegnen, geschehen geheimnisvolle Dinge, denen wir in diesem Beitrag auf den Grund gehen. Denn die Pot Still ist weit mehr als ein physikalischer Trennapparat. In ihr entfaltet sich ein wahres Aromen-Spektakel. Sprich: unerwünschte Stoffe verschwinden, neue Aromen entstehen – es wird dort bereits das facettenreiche Fundament für den späteren Whisky gelegt, noch bevor ein Fass ins Spiel kommt. Es ist das Zusammenspiel von Hitze, Kupfer und Moleküle, die das Destillat veredeln. Willkommen im innersten Labor der Whiskyherstellung!
Destillation – mehr als nur Trennung
Am Anfang steht die Wash, eine bierartige Flüssigkeit mit rund 7-10 Prozent Alkohol. In der Pot Still wird sie erhitzt – und genau hier kommt es zur klassischen Trennung: Alkohol verdampft bei niedrigeren Temperaturen als Wasser, steigt als Dampf auf, wird kondensiert und gesammelt. Nach zwei Durchläufen – zunächst in der Wash Still, dann in der Spirit Still – bleibt der sogenannte Mittellauf, auch „Hearts“ genannt. Mit weit über 60 Prozent Vol. Alkohol ist er das Herzstück für die spätere Reifung im Eichenfass.
Doch was sich im Inneren der Brennblase abspielt, ist weit mehr als nur reine Physik. Hier beginnt die Magie der Aromen.
Kupfer – der stille Held des guten Geschmacks
Wer je eine Pot Still gesehen hat, weiß: Kupfer (Cu) ist das dominierende Material in klassischen Brennblasen. Das rotgolden glänzende Metall ist nicht nur wegen seiner guten Wärmeleitfähigkeit beliebt – es ist chemisch hochaktiv. Kupfer bindet schwefelhaltige Verbindungen, die beim Gären durch schwefelhaltige Aminosäuren, wie Cystein und Methionin, entstehen und die an faule Eier, gekochtes Gemüse oder gar Schlimmeres erinnern – alles andere als ein Genuss! Beispiele dafür sind Schwefelwasserstoff (H₂S), Schwefeldioxid (SO2), Ethanthiol (C2H5SH), Dimethylsulfid (DMS), Dimethyldisulfid (DMDS) und Dimethyltrisulfid (DMTS). Diese Stoffe werden olfaktorisch entschärft, indem sie mit der Kupferoberfläche zu schwerflüchtigen Kupfersulfiden oder Kupferkomplexen reagieren. Diese Salze lagern sich in der Brennblase ab und gehen nicht ins Destillat über.
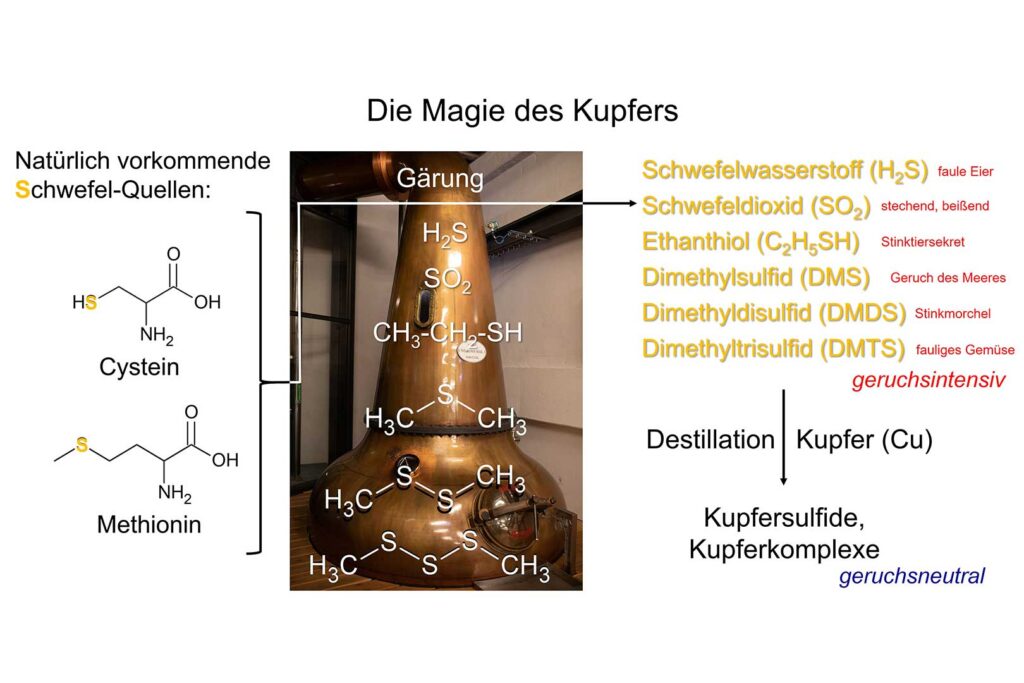
Je länger der Dampf mit Kupfer in Kontakt bleibt – etwa bei langsamer Destillation oder langen Brennblasen – desto intensiver ist dieser reinigende Effekt. Das Resultat: ein klareres, eleganteres Destillat mit weniger störenden Schwefelnoten.
Wie Schwefelaromen trotzdem entstehen – und manchmal sogar gewollt sind
Wissenschaftlich betrachtet ist die Welt der Schwefelverbindungen äußerst komplex. Manche entstehen erst während der Destillation durch Hitze – andere zerfallen oder verändern sich. In Studien konnte festgestellt werden, dass Dimethyldisulfid (DMDS) und DMTS während des Destillationsprozesses zunehmen und durch höhere Temperaturen und längere Destillationszeiten sogar begünstigt werden. Einige dieser Schwefelverbindungen, in kleinsten Mengen, können den Whisky jedoch bereichern – vor allem bei getorften Whiskys, wo sie würzige oder rauchige Tiefe verleihen.
Wie so oft gilt: Die Dosis macht den Unterschied.
Reaktionen im Gleichgewicht – ein Molekül kommt selten allein
Manche der chemischen Reaktionen in der Brennblase verlaufen nicht einfach „von A nach B“, sondern stellen ein Gleichgewicht her – dargestellt durch den Doppelpfeil (⇌). Das bedeutet: Die Reaktion kann prinzipiell in beide Richtungen ablaufen. Entscheidend sind dabei die Bedingungen, wie Temperatur, Alkoholgehalt oder Wasseranteil. In der Praxis verschiebt sich das Gleichgewicht meist deutlich zugunsten der gewünschten Aromen – ein Glücksfall für den späteren Whisky.
Säuren und Alkohole – wenn Ester das Aromabild prägen
Neben diesen Reinigungsprozessen spielt sich noch ein weiteres chemisches Schauspiel ab: die sogenannte Veresterung. Dabei reagieren Alkohole – allen voran Ethanol – mit organischen Säuren zu Estern, also Duftstoffen, die oft fruchtige Akzente setzen. Sie prägen das Aromabild vieler Whiskys – etwa Banane (Isoamylacetat), Apfel (Ethylacetat) oder Birne (Propylacetat)“:
Säure + Alkohol ⇌ Ester + Wasser
Die Vielfalt der vorhandenen Alkohole und Säuren führt dabei zu einer komplexen Mischung an Estern, die den Charakter des späteren Whiskys grundlegend (mit) prägen.
Die Um-Esterung: Umgruppierung im heißen Dampf
Tatsächlich kann es während der Destillation auch zur Um-Esterung kommen – also zur Umwandlung eines vorhandenen Esters in einen neuen durch Austausch der Alkohol- oder Säuregruppe. Diese Um-Esterung verläuft unter Hitzeeinwirkung und in alkoholischer Umgebung besonders effizient. Beispiel:
Ethylacetat + Isoamylalkohol ⇌ Isoamylacetat + Ethanol
Das Ergebnis: ein sich während der Destillation dynamisch veränderndes Esterprofil – ein unsichtbares Spiel der Moleküle, das zur späteren Komplexität beiträgt.
Acetal-Bildung – florale und süße Akzente
Im dampfenden Alkoholgemisch können sich Aldehyde (reaktionsfreudige Zwischenprodukte, die zum Beispiel beim Abbau von Zucker entstehen) mit Alkoholen zu sogenannten Halb-Acetalen und Acetalen verbinden – Verbindungen, die für ihre floralen und süßlichen Aromen bekannt sind:
Acetaldehyd + Ethanol ⇌ 1-Ethoxyethanol (ein Halb-Acetal)
Acetaldehyd + 2 Ethanol ⇌ 1,1-Diethoxyethan (ein Acetal)
Diese Acetale bringen florale oder süßliche Noten ins Destillat, erinnern an Wein oder Honig – kleine, feine Nuancen, die in Summe zur Eleganz beitragen.
Spezialfall: Direkt befeuerte Brennblasen
Die meisten schottischen Brennereien nutzen heute indirekte Dampferhitzung, bei der die Wash gleichmäßig auf etwa 100 °C gebracht wird. Einige wenige – darunter Springbank oder Glenfarclas – setzen weiterhin auf die direkte Befeuerung ihrer Pot Stills mit Gas oder offenem Feuer.
Was archaisch anmutet, hat einen entscheidenden Effekt: lokale Hitzespots am Kupferboden der Brennblase. Dort kann die Temperatur auf weit über 150 °C steigen – besonders, wenn sich Rückstände wie Zucker, Aminosäuren oder Hefepartikel ablagern und anbrennen.
Und genau hier wird es chemisch besonders spannend:
Maillard-Reaktionen
Wo Zucker und Aminosäuren bei Hitze zusammentreffen, kann es zur Maillard-Reaktion kommen – jener komplexen, nicht-enzymatischen Bräunungsreaktion, die auch beim Rösten von Brot oder Braten von Fleisch für die typische Farbe und den herzhaften Duft sorgt. Das Ergebnis: malzige, brotartige, leicht fleischige Aromen, die später Tiefe verleihen.
Karamellisierung
Auch Zucker selbst kann bei diesen Temperaturen karamellisieren. Durch die Reaktion von Zucker mit Zucker, die ohne Beteiligung von Aminosäuren abläuft, entstehen süßlich-bittere Aromen wie Furanone oder HMF (5-Hydroxymethylfurfural), die an geröstete Nüsse, Mandeln oder gebräunten Zucker erinnern.
Strecker-Abbau
Im Zusammenspiel mit der Maillard-Reaktion kann es zum sogenannten Strecker-Abbau von Aminosäuren kommen, benannt nach dem deutschen Chemiker Adolph Strecker. Dies ist ein Prozess, bei dem durch Hitze kleine, aromatisch wirksame Moleküle entstehen, wie zum Beispiel Methional (gekochte Kartoffel), Isovaleraldehyd (malzig, nussig) oder Phenylacetaldehyd (blumig, honigartig). Diese zählen zu den sogenannten Aldehyden, die stark am Aroma mitwirken.
Aromatischer Einfluss
Was die direkte Befeuerung auszeichnet? Kräftigere, würzigere, tiefgründigere Destillate, die in der Fassreifung besonders komplexe Aromen entfalten können. In der Hand erfahrener Brennmeister wird das Feuer zum Instrument – bewusst gesteuert für mehr Charakter.
Hitze als Katalysator des Aromas
Was all diese Prozesse verbindet, ist die hohe Temperatur innerhalb der Pot Still. Sie setzt chemische Prozesse in Gang, die bei Raumtemperatur kaum oder gar nicht ablaufen würden. So wird aus der Brennblase ein aromatisches Labor, in dem das spätere Geschmacksprofil schon vor dem Holzfass vorbereitet wird.
Fazit: Die Brennblase als Alchemistin
Während der Destillation findet weit mehr statt als bloßes „Verdampfen und Auffangen“. In der Pot Still laufen eine Vielzahl von chemischen Reaktionen ab – manche helfen, unerwünschte Aromen zu entfernen, andere tragen direkt oder indirekt zur Komplexität des Whiskys bei. Die Brennblase trennt nicht nur – sie gestaltet, veredelt und komponiert das sensorische Fundament.
Wer sich tiefer mit der Whiskyproduktion beschäftigt, erkennt: Whisky entsteht nicht allein im Fass, sondern beginnt bereits mit Hitze, Metall und Molekülen im Herzen der Brennblase.