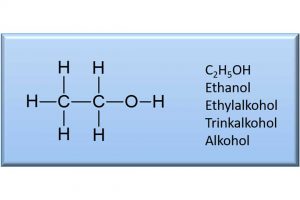
Nein – unser vertrautes Ethanol hat keine weibliche Bekanntschaft gemacht. Mit Ester ist also nicht ein Frauenname gemeint, sondern – und Sie, verehrte Leserschaft, sollten mich mittlerweile schon so gut kennen – es handelt sich bei Ester um eine chemische Verbindungsklasse. Natürlich, was denn sonst?! Aber, es ist eine Substanzklasse, die es in sich hat!
Betörende Fruchtnoten
Lieben Sie das auch? Ich meine, die ausgeprägte Fruchtigkeit, die viele Whiskys im Aroma und im Geschmack aufweisen? Gerade bei solchen, die aus der Speyside stammen – Schottlands größter Whiskyregion, was die Anzahl der Destillerien anbelangt. Bei ihnen dominieren oft die fruchtigen Aromen, die von Beeren (Brombeere, Erdbeere, Stachelbeere) und Obst (Birne, Apfel, Aprikose, Pfirsich) über exotische Früchte (Ananas, Mango, Banane) bis hin zu Gewürzen (Anis, Gewürznelke, Zimt) reichen können. Ich finde diese Aromavielfalt betörend und könnte stundenlang an so einem fruchtbetonten Whisky riechen. Kein Wunder, wenn es nämlich darum geht, einen Whisky sensorisch zu beschreiben, sind fruchtige Noten mit die am einfachsten zu erkennenden Aroma- und Geschmacksrichtungen. Doch welche Stoffe sind dafür verantwortlich? Und woher stammen diese? Einige Verbindungen, die hier zu nennen wären, habe ich Ihnen bereits in Teil 5 unserer Reihe vorgestellt. Doch nun ist es notwendig, noch tiefer in die Materie einzutauchen. Um dies zu verstehen, müssen wir Ihre mutmaßlich etwas verstaubten Chemiekenntnisse aus der Schule wieder auffrischen. Doch keine Angst, ich helfe Ihnen dabei!
Ester – eine wichtige Substanzklasse
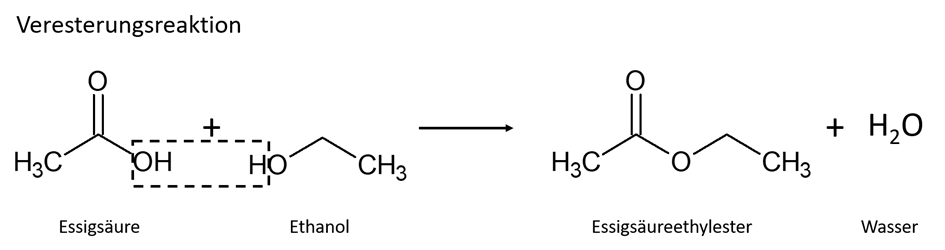
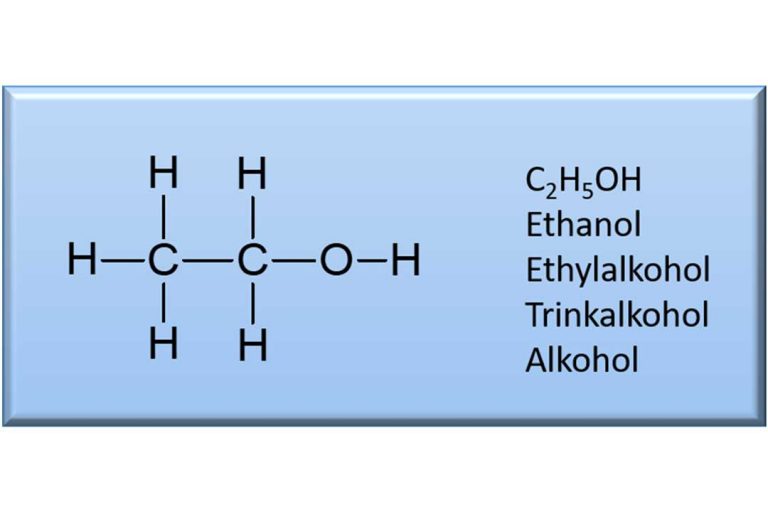
Was sind also Ester? Was verbirgt sich hinter diesem chemischen Begriff? Nun, Ester verkörpern eine chemische Substanzklasse aus dem Bereich der organischen Chemie. Sie werden aus Säuren und Alkoholen gebildet. Nur zwei Stoffe also. Man kann sich Ester wie einen Zwei-Komponenten-Kleber vorstellen. Man hat auf der einen Seite eine Säure. Beispielsweise die Essigsäure, die wir als sauren Bestandteil des Essigs kennen. Auf der anderen Seite haben wir einen Alkohol, wie z. B. unser mittlerweile lieb gewonnenes Ethanol. Fügt man also – bildlich gesprochen – eine Säure mit einem Alkohol zusammen, dann „kleben“ die beiden aneinander fest, Wasser wird abgespalten und das neue Molekül „härtet“ dadurch aus. Es entsteht auf diese Weise eine neue Verbindung, bei der ein Teil der Säure mit einem Teil des Alkohols zusammengeklebt und Wasser entfernt wurde. Diese neue Verbindungsklasse nennen wir Chemiker Ester. Ein Ester entsteht also immer durch die Reaktion einer Säure mit einem Alkohol unter Abspaltung von Wasser! Eigentlich ganz simpel, oder?
Die Dinge beim Namen nennen
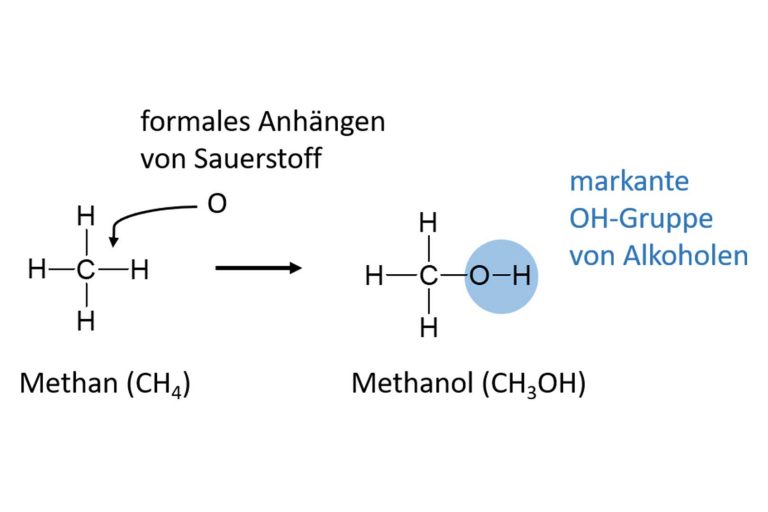
In unserem Beispiel wird aus der Essigsäure und dem Ethanol der Ester „Essigsäureethylester“ gebildet. Zugegeben, die Bezeichnung – die Nomenklatur – ist etwas diffizil. Aber nur auf den ersten Blick. Denn in der Benennung der Ester bleibt der Name der Säure bestehen. Nur der Name des Alkohols verändert sich. Aus Ethanol wird „Ethyl“. Man lässt einfach den Teil „anol“ weg und fügt stattdessen „yl“ daran. Und zum Schluss hängt man dann noch die Endung „ester“ an das Wort und schon ist der chemische Name für den Ester perfekt. Probieren wir es gleich aus. Aus Essigsäure und Ethanol wird Essigsäureethylester. Gut, das steht ja auch schon ein paar Zeilen darüber. Machen wir noch ein Beispiel: Wie heißt der Ester aus Essigsäure und Methanol? Der Säurename bleibt gleich, aus Methanol wird „methyl“ und am Ende kommt noch „ester“ hinzu. Heißt also: Essigsäuremethylester. Und der Ester aus Propansäure und Butanol? Wieder bleibt die Säure gleich und aus Butanol wird „butyl“. Fertig ist der Ester: Propansäurebutylester. Jetzt ist bestimmt auch der letzte Zweifler und die letzte Zweiflerin überzeugt, dass Chemie wirklich einfach ist, oder?!
Wo werden Ester gebildet?
Da wir jetzt wissen, wie Ester gebildet werden, interessiert uns noch die Frage, woher sie beim Herstellungsprozess von Whisky stammen. Die Ester bilden sich hauptsächlich während der alkoholischen Gärung. Also dem Prozessschritt, in dem die Hefe Zucker in Ethanol umwandelt. Es wurden über 100 verschiedene Ester identifiziert, die während der Gärung entstanden sind, wobei in der Regel längere Gärzeiten zu mehr Estern führen. Doch die Gärung ist nicht die einzige Bildungsquelle. Ester entstehen auch während der Destillation in den kupfernen Pot Stills. Und zwar dann, wenn sich flüchtige Säuren und Alkohole in den aufsteigenden Dämpfen auf der inneren Kupferoberfläche treffen und miteinander reagieren. Zu guter Letzt werden die Ester auch während der Reifung im Eichenfass aus den unterschiedlichen Säuren und Alkoholen, die die Hefe während der alkoholischen Gärung produzierte, gebildet. Der am häufigsten gefundene Ester im Whisky ist der bereits angesprochene Essigsäureethylester. Dieser wird kontinuierlich im Fass gebildet und seine Konzentration steigt dadurch stetig im Laufe der Jahre im Fass an. Somit ist diese chemische Verbindung ein Indikator, ein Maß für die Reifung. Während Essigsäureethylester in geringer Konzentration ein fruchtiges, an grüne Äpfel erinnerndes Aroma besitzt, kann mit zunehmendem Alter des reifenden Destillats die Menge an diesem Ester einen Bereich erreichen, bei dem ein unangenehmer Geruch nach Klebstoff entsteht.
Rumaroma
Es ist schon erstaunlich, wie sich die Eigenschaften einer Säure verändern, wenn sie mit einem Alkohol zu einem Ester reagiert. Fangen wir mit der Ameisensäure an. Sie alle kennen diese Verbindung und sind bestimmt schon das ein oder andere Mal mit ihr in Berührung gekommen. Denn diese farblose und ätzende Flüssigkeit wird in der Natur von kleinen schwarzen oder roten Lebewesen – den Ameisen – zu Verteidigungszwecken genutzt. Daher auch der Trivialname Ameisensäure, die eigentlich Methansäure heißt. Bringt man diese ätzende Chemikalie mit unserem Alkohol Ethanol zur Reaktion, so entsteht – richtig, Sie sind ja mittlerweile fit in der chemischen Nomenklatur der Ester – Ameisensäureethylester. Ein Ester mit einem ausgeprägten Aroma nach Rum bzw. Arrak! Wow – ist das nicht verblüffend? Ich meine ja. Aber es geht noch spektakulärer! Und dazu möchte ich Ihnen eine kleine Geschichte erzählen.
Aus eklig mach fruchtig
Vor einigen Jahren kam meine Tochter aufgeregt von der Schule, sah mich mit einem entsetzten Gesichtsausdruck an und fragte mich in einem fast schon verzweifelten Tonfall: „Papa, hast du schon mal Buttersäure gerochen?“ Meine Anspannung löste sich sogleich und ich antwortete vielsagend: „Oh ja!“ „Bah, ist das ein ekliges Zeug!“, ereiferte sich meine Tochter. „Das riecht wie saure Milch, wie penetranter Schweiß oder ranzige Butter!“ „Aber nur im günstigsten Fall“, entgegnete ich. „Ja, und eigentlich riecht es wie frisch Erbrochenes“, resümierte sie. „Jetzt kommen wir der Sache schon näher“, schlussfolgerte ich. „Um Himmelswillen, was habt ihr denn in der Schule angestellt?“, fragte ich. „Hat irgendjemand von euch ein paar Tropfen von dieser farblosen, leicht öligen Flüssigkeit im Turnraum versprüht und jetzt habt ihr zwei Wochen keinen Sport mehr?“, fragte ich. „Nein“, antwortete sie, „wir haben einen Versuch gemacht, in Chemie.“ „Oh, das ist ja interessant“, bemerkte ich höchst erfreut. „Was habt ihr denn gemacht?“, wollte ich wissen. „Wir haben eine Veresterungsreaktion gemacht! Weißt du was das ist?“, fragte sie mich. „Ich habe keine Ahnung“, flunkerte ich. „Stell dir vor: wir nahmen dieses eklige Zeug, diese Buttersäure, und gaben Ethanol hinzu. Einen Alkohol, kennst du den?“, fragte sie mich. „Habe ich schon mal von gehört“, antwortete ich augenzwinkernd. „Also“, fuhr sie fort, „Wir nahmen also diese eklig riechende Buttersäure, gaben Ethanol und ein paar Tropfen konzentrierte Schwefelsäure dazu, als Katalysator, weißt du?“. Ich nickte. „Und dann machten wir die Veresterungsreaktion. Weißt du, was dann herauskam?“, fragte sie mich. „Nee, erzähl mal“, gab ich mich ahnungslos. „Da kam eine Verbindung heraus, die roch ungefähr so, als wenn man eine frische Tüte Tropifrutti öffnet und tief hineinriecht. Es roch nach tropischen Früchten, hauptsächlich nach Ananas!“, sagte sie mit einem begeisterten Gesichtsausdruck. Und ganz genau das ist passiert. Buttersäure reagiert mit Ethanol zu der Verbindung Buttersäureethylester, welche ein intensives Ananasaroma aufweist. Da soll noch einer sagen, Chemie wäre langweilig!
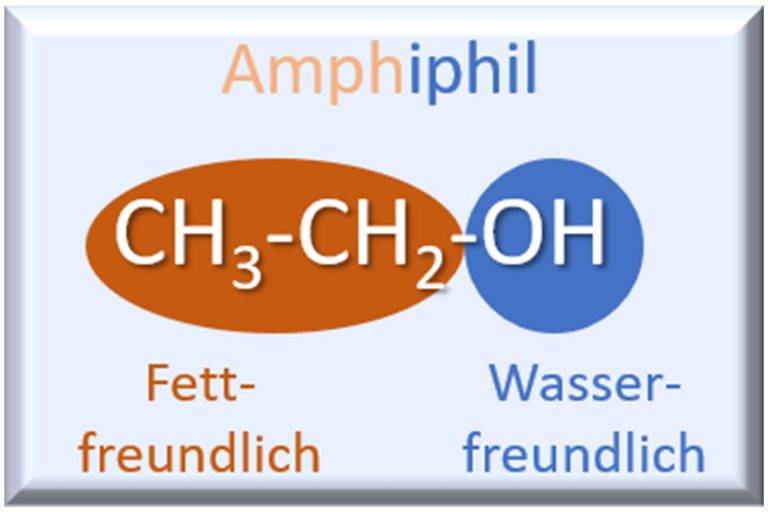
Es ist schon erstaunlich. Ethanol ist nicht nur die Basis unserer begehrten Spirituose Whisky, sondern hat als amphiphile Verbindung (siehe Teil 3 unserer Reihe) sowie als Lösungsmittel interessante und wichtige Eigenschaften. Und nun fungiert es auch noch als Reaktionspartner für Säuren, um dem Whisky die fruchtigen Aromen zu verleihen, die ich und mit Sicherheit auch Sie, liebe Leserschaft, so sehr begehren.